Arixtra
Säkerhetsprofil
Biverkningar, kontraindikationer1
De vanligaste rapporterade, allvarliga biverkningarna med fondaparinux är blödningskomplikationer (olika blödningsställen inklusive sällsynta fall av intrakraniell/intracerebral och retroperitoneal blödning) och anemi.
- Fondaparinux ska användas med försiktighet hos patienter med ökad blödningsbenägenhet.
- Fondaparinux är endast avsett för subkutan injektion och ska inte administreras intramuskulärt.
Biverkningarna i tabellen nedan anges efter organsystemklass och frekvens. Frekvenserna definieras som mycket vanliga (≥ 1/10), vanliga (≥ 1/100, < 1/10), mindre vanliga (≥ 1/1 000, < 1/100), sällsynta (≥ 1/10 000, < 1/1 000) och mycket sällsynta (< 1/10 000).
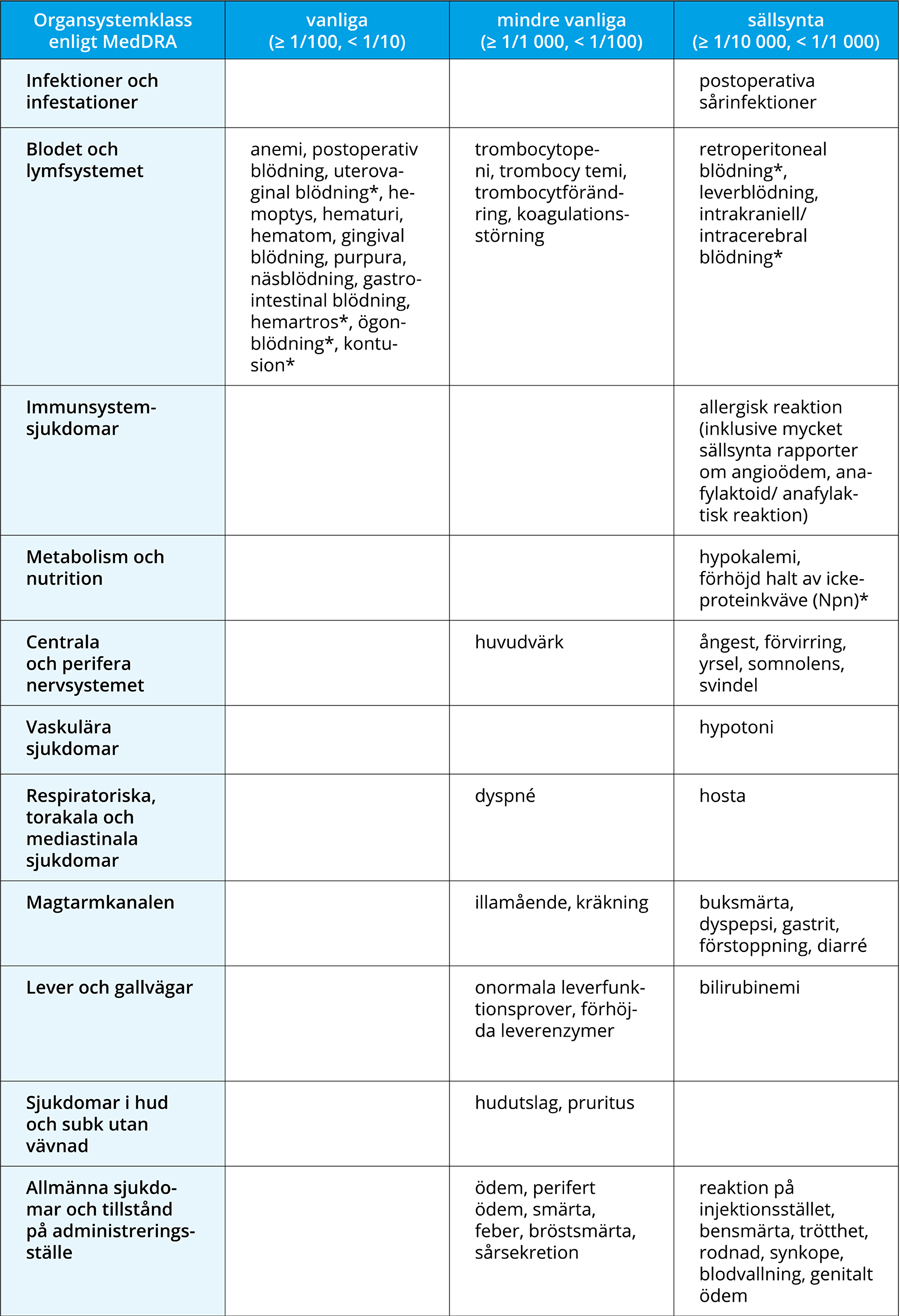
Npn = icke-proteinkväve som urea, urinsyra, aminosyra osv.
* Biverkningarna inträffade vid högre doser: 5 mg/0,4 ml, 7,5 mg/0,6 ml och 10 mg/0,8 ml.
För biverkningar hos patienter som genomgår större ortopedisk kirurgi i de nedre extremiteterna och/eller bukkirurgi se Arixtra® produktresumé.
Kontraindikationer, varningar och försiktighetsåtgärder1
Kontraindikationer
- Överkänslighet mot den aktiva substansen eller mot något hjälpämne
- Pågående kliniskt signifikant blödning
- Akut bakteriell endokardit
- Kraftigt nedsatt njurfunktion
Särskilda varningar
För användning av Arixtra® i följande situationer, se den fullständiga förskrivningsinformationen.
- Äldre patienter
- Försämrad njurfunktion
- Kraftigt nedsatt leverfunktion
- Låg kroppsvikt
- Patienter med ökad blödningsrisk
- Spinal- och epiduralanestesi
- Latexallergi
- Patienter med anamnes på heparininducerad trombocytopeni
- Samtidig användning av läkemedel som ökar risken för blödning
För mer information om kontraindikationer, särskilda varningar och fertilitet, graviditet och amning, se förskrivarinformationen för Arixtra®.
Arixtra®(fondaparinux) Rx. Ff (vissa förpackningar är subventionerade). ATC: B01AX05. Injektionsvätska i förfyllda sprutor: 7,5 mg/0,6 ml, 2,5 mg/0,5 ml och 1,5 mg/0,3 ml. Arixtra 2,5 mg och Arixtra 1,5 mg har indikation behandling av vuxna med akut symtomgivande spontan ytlig ventrombos i de nedre extremiteterna utan samtidig djup ventrombos. Profylax av venös tromboembolisk sjukdom hos vuxna som genomgår större ortopedisk kirurgi i de nedre extremiteterna eller bukkirurgi samt vid immobilisering p.g.a. akut sjukdom. Arixtra 2,5 mg har även indikation behandling av instabil angina, icke-ST-höjningsinfarkt (UA/NSTEMI) och ST-höjninginfarkt (STEMI) hos vuxna. Arixtra 7,5 mg är indicerat vid akut behandling av vuxna med akut djup ventrombos och behandling av akut lungemboli, med undantag för hemodynamiskt instabila patienter eller patienter i behov av trombolys eller embolektomi. Kontraindicerat vid: pågående kliniskt signifikant blödning, akut bakteriell endokardit, kraftigt nedsatt njurfunktion (kreatininclearance <20 ml/min). Skall ej administreras intramuskulärt. Skall användas med försiktighet hos patienter med ökad blödningsbenägenhet. Fondaparinux ska användas under graviditet endast då det är absolut nödvändigt. Amning rekommenderas ej under behandling med fondaparinux. Produktresumén senast uppdaterad: 10-2024. För ytterligare information och priser se fass.se. Viatris AB Tel: 08-630 19 00.
Referencer:
- Arixtra® produktresumé, senast uppdaterad 10-2024, fass.se https://www.fass.se/LIF/result?query=arixtra&userType=0
SE-ARX-2025-00035 Sep
Innehåll
Utbildningsmaterial
Diagnos & behandling av ytlig ventrombos. Föreläsare: Mazdak Tavoly, Med Dr, Överläkare. Sahlgrenska Universitetssjukhuset