Creon
Creon effekt, säkerhet och tolerabilitet
Totalt har 30 studier genomförts som undersöker effekten av Creon hos patienter med exokrin pankreasinsufficiens. Tio av dessa var placebokontrollerade studier som utfördes på patienter med cystisk fibros, kronisk pankreatit eller postoperativa tillstånd.7
Creon vid kronisk pankreatit
Creon har visat sig förbättra symtomen hos patienter med kronisk pankreatit och exokrin pankreasinsufficiens (EPI).8
Creon förbättrar symtom som förknippas med EPI8:
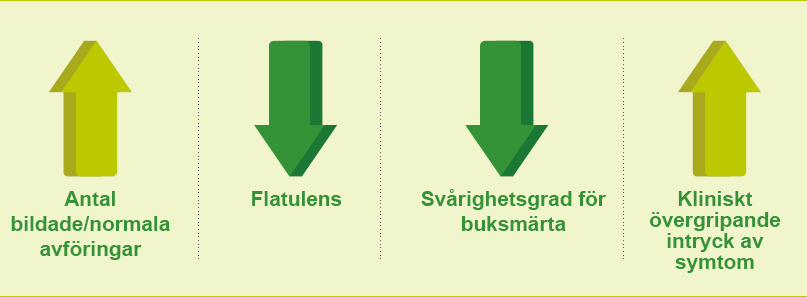
Creon förbättrar fettabsorptionen hos patienter med EPI efter pankreaskirurgi:9
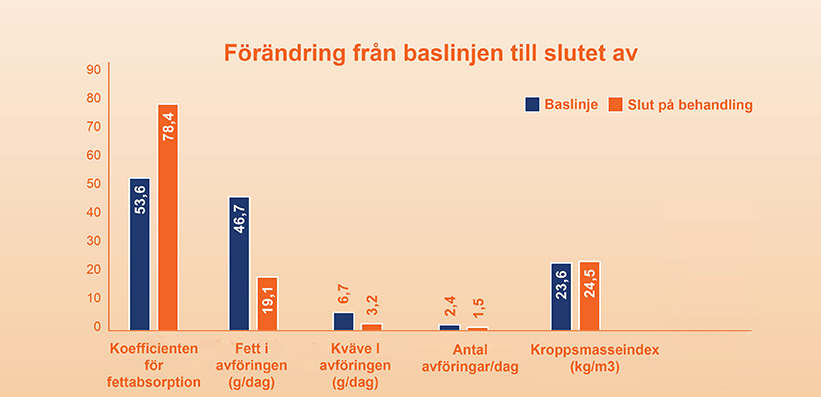
Förändring från baslinjen till slutet av den öppna förlängningsperioden 9
Creon tolererades väl, utan några seriebiverkningar eller biverkningar som ledde till avbrott under den randomiserade perioden.9
Utformning av Seiler-studien9: En 1 vecka lång, dubbelblind, randomiserad, placebokontrollerad multicenterstudie med parallella grupper och en ettårig öppen förlängning (OLE). Patienter ≥18 år med exokrin pankreasinsufficiens efter pankreasresektion, definierad som baslinjekoefficient för fettabsorption (CFA) <80 %, randomiserades till Creon eller placebo (9–15 kapslar/dag: tre med huvudmåltider, två med mellanmål). I den öppna förlängningen (OLE) fick alla patienter Creon.
Creon vid cystisk fibros
Creon signifikant förbättring av CFA hos patienter med EPI på grund av cystisk fibros i åldern 12 till år:13
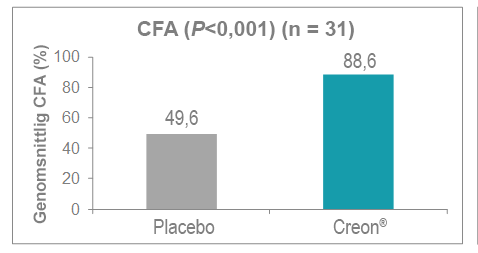
Förbättring av CFA-diagram 8.
De vanligaste behandlingsrelaterade biverkningarna (TEAE) som rapporterades i Trapnell-studien var gastrointestinal-relaterade, yrsel och hosta.
Analys av biverkningar visade inga TEAE med en kliniskt meningsfullt större incidens i Creon-gruppen jämfört med placebogruppen, och inga fall av överkänslighet rapporterades.13
Trapnell-studiens utformning: 13
Randomiserad, dubbelblind, multicenter, placebokontrollerad, 2-periods crossoverstudie av CREON hos 32 patienter i åldern 12 till 43 år med bekräftad diagnos på EPI och CF. Patienterna randomiserades till att få CREON 24 000 lipaskapslar med en måldos på 4 000 lipasenheter per gram fett per dag, eller matchande placebo i 5 till 6 dagar, följt av övergång till den alternativa behandlingen i 5 till 6 dagar. En washout-period på 3 till 14 dagar inkluderades mellan crossover-perioder för att återföra patienter till baslinjeförhållanden. Det primära effektmåttet var koefficienten för fettabsorption (CFA) och det sekundära effektmåttet var koefficienten för kväveabsorption (CNA). Den slutliga analyspopulationen var begränsad till 29 patienter; 3 patienter uteslöts på grund av protokollavvikelser.
Creon kapslar (pankreatin) är ett receptfritt läkemedel som används vid behandling av otillräcklig funktion hos bukspottkörteln (exokrin pankreasinsufficiens) med bristfälligt upptag av näringsämnen från tarmen. Dosen bestäms av behandlande läkare och anpassas individuellt beroende på sjukdomens allvarlighetsgrad samt kostens sammansättning. Läs bipacksedeln noga före användning. Bipacksedeln uppdaterades senast: 2022-12-27 och 2022-12-28. Marknadsförs av BGP Products AB (A Viatris Company) 08-630 19 00.
Referencer:
- Internal calculations by Mylan, IQVIA database, Midas database, IQVIA Midas worldwide value and volume Q2 2019.
- Data on file. Pancreatin Cumulative Patient Exposure Report, Review Period: 14-April 1980 to 22-April 2019.
- Whitcomb D, et al. Pancrelipase Delayed-Release Capsules (CREON) for Exocrine Pancreatic Insufficiency due to Chronic Pancreatitis or Pancreatic Surgery: A Double-Blind Randomized Trial. Am J Gasteoenterol.2010;105:2276-2286.
- Ramesh H, et al. A 51-week, open-label clinical trial in India to assess the efficacy and safety of pancreatin 40000 enteric-coated minimicrospheres in patients with pancreatic exocrine insufficiency due to chronic Pancreatitis. Pancreatology 2013; 13:133-139.
- Thorat V, et al. Randomized clinical trial: the efficacy and safety of pancreatin enteric-coated minimicrospheres (Creon 40000 MMS) in patients with pancreatic exocrine insufficiency due to chronic pancreatitis – a double-blind, placebo-controlled study. Aliment Pharmaco Ther. 2012;36:424-436.
- Seiler CM et al. Randomized clinical trial: a 1-week, double-blind, placebo-controlled study of pancreatin 25.000 Ph. Eur. Minimicrospheres (Creon 25.000 MMS) for pancreatic exocrine insufficiency after a pancreatic surgery, with a 1-year opne-label extension. Aliment Pharmaco Ther. 2013;37:691-702.
- Creon 25 000 produktresumé 2022 Dec, hämtad från: https://www.fass.se/LIF/product?userType=0&nplId=19910705000053&docType=6&scrollPosition=0
- Ramesh H et al. A 51-week, open-label clinical trial in India to assess the efficacy and safety of pancreatin 40000 enteric-coated minimicrospheres in patients with pancreatic exocrine insufficiency due to chronic pancreatitis. Pancreatology, 2013; 13:133-139.
- Seiler CM, et al. Randomised clinical trial: A1-week, double-blind, placebo-controlled study of pancreatin 25 000 Ph. Eur. Minimicrospheres (Creon 25000 MMS) for pancreatic exocrine insufficiency after pancreatic surgery, with a 1-year open-label extension. Aliment Pharmacol Ther. 2013; 37:691–702.
- Trapnell BC, et al. Efficacy and safety of CREON 24,000 in subjects with exocrine pancreatic insufficiency due to cystic fibrosis.J Cyst Fibros 2009;8(6):370–377